ハンドウイルカの尿性状
2014.02.24 up
2009年1月
展示課 新田 誠
海洋哺乳動物の生物学的試料の採取並びに検査は,海洋という特殊な環境に進出した哺乳類の高浸透圧環境への適応進化の解明に役立ち,飼育下の動物の生理学研究や健康管理に有用です。しかし,水中生活に適応したクジラ目の場合,身体の拘束による試料の採取や病気の治療には危険が伴い,必ず必要とする試料が得られるとは限りません。新潟市水族館マリンピア日本海では,飼育下,クジラ目に,正の強化を用いたオペラント条件付けを応用し,身体的拘束をすることなく,身体検査や治療,さらには生物学的試料の採取を安全に実施するための行動形成を行っています.行動形成による生物学的試料の採取は,トレーナーと動物の双方に危険が及ぶことを極力回避でき,また,採取手続きに掛かる人手や時間が簡略化されることから,継続的な試料採取が可能となります。
本研究の対象とした尿は,非侵害的に得ることができ,比較的容易に病気の種類や程度・活動性などを知ることができます。
当館では,尿検査を飼育動物の生理値の解明および健康診断の指標とする目的で,飼育下クジラ目の尿を週1回の頻度で定期的に採取してきました。
約1年間の尿を採取し検査した結果,メスのハンドウイルカ5頭(個体C:飼育年数15年,K・Y:13年,R・A:3年)の尿性状について,若干の知見が得られました。
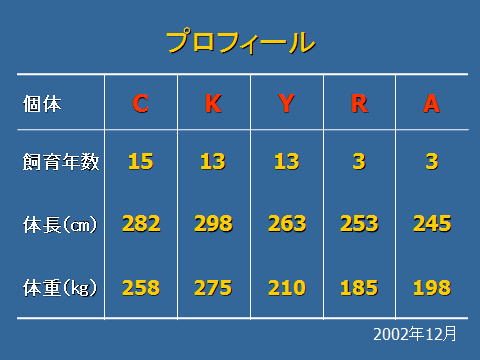
採尿期間は、個体C,K,Yが,2001年12月6日~2002年11月27日までの約1年間,個体R,Aは,2002年5月15日~11月27日までの約半年間であり,201検体の尿サンプルが得られました。
採尿方法は,①腹部をトレーナー側に向けてステージに上げ,自発的な排尿を待ちます。②体側に付着した海水の混入を防ぐため,生殖溝
付近の海水をタオルで拭き取ります。③生殖溝付近を観察し,排尿を視認します。④排尿後,すぐさま用意していた容器で採取します。




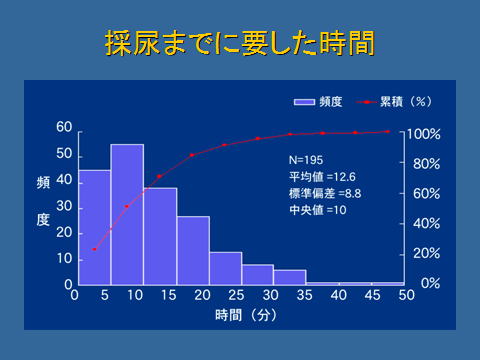
排尿までに要した時間は,最短で1分,最長で50分です。5~10分が最も多く,中央値は10分でした。
検査項目は,物理的検査,化学的検査,沈渣の鏡検,非電解質および電解質濃度の大きく分けて,4つの項目であり,計19項目について測定を行いました。
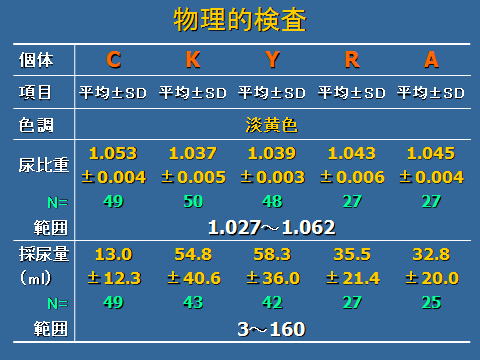
尿の色調は,201検体すべて淡黄色でしたが,検体ごとに若干の濃淡のあることが確認されました。


採尿量の測定には,メスシリンダーを使用し,尿比重の測定には,尿検査用の尿比重屈折計(ユリコンJE,アタゴ社)を使用しました。
物理的検査の結果,尿比重の範囲は,1.027~1.062でした。採尿量は,すべての尿の採取はできませんが,最大で160mlでした。
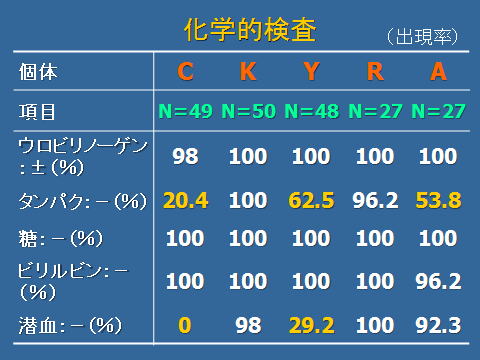
化学的検査の結果,pHの範囲は,5.0~7.5,ウロビリノーゲン,±~+タンパク,-~+糖-ビリルビン,-~±,潜血,-~++でした。
ウロビリノーゲン~潜血については,異常値も得られたため,個体ごとの出現率を調査した結果,タンパクと潜血に異常値の出現が比較的多く見られ,個体Cと個体Yに潜血反応が頻繁に見られました。

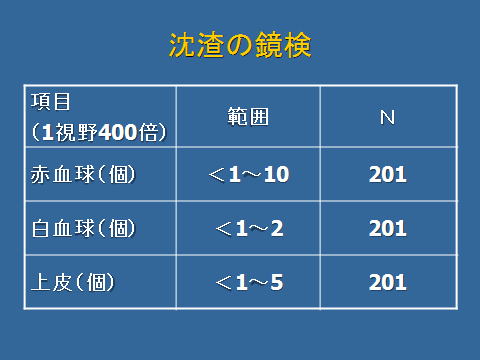
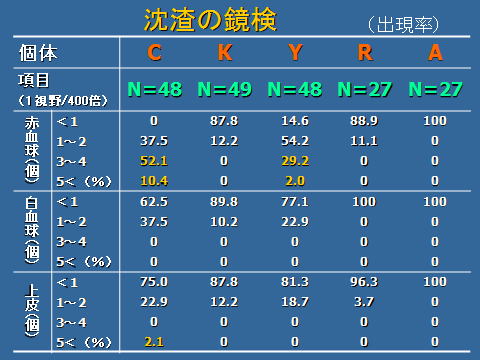
沈渣を鏡検した結果,赤血球と上皮が通常より多く見られた検体がありました。通常,赤血球,白血球,上皮は,400倍1視野で,1未満~2個程度見られます。個体ごとに出現した赤血球,白血球,上皮を4つの区間に区切り,出現率を調べた結果,個体Cで全体の約60%,個体Yで全体の約30%の割合で尿中の赤血球増加が見られ,5個以上が,それぞれ約10%と2%みられました。

非電解質および電解質濃度を測定した結果,尿素窒素の範囲は,844~3123㎎/dl,クレアチニンの範囲は,28.7~192.5㎎/dl,浸透圧の範囲は,844~3123 mOsm/㎏,Naの範囲は,165~620 mEq/l,Kの範囲は,32.5~166 mEq/l,Clの範囲は,205~620 mEq/l,Caの範囲は,0.3~35㎎/dl,Mgの範囲は,2.0~16.5㎎/dl,Pの範囲は,20.1~185㎎/dlでした。
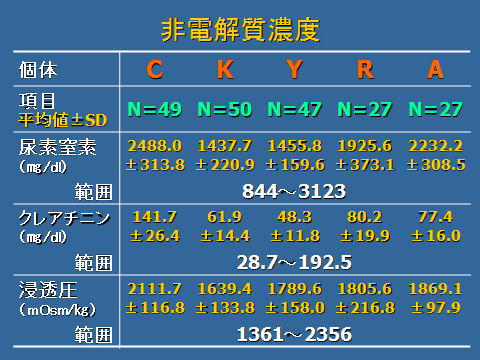
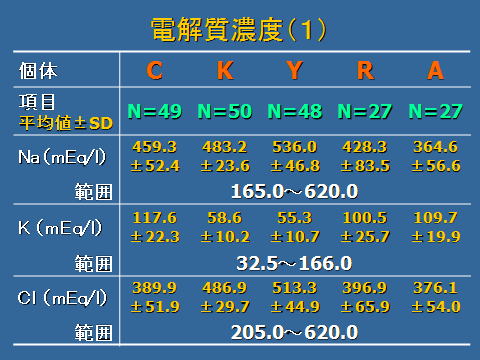
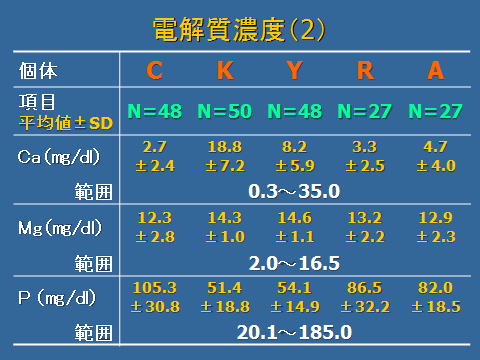
尿比重,尿素窒素,クレアチニン,浸透圧,電解質濃度について,各個体間の平均値の差異を,t検定により検討し検出した結果,有意水準1%で各項目に有意な差が多く見られ,尿の比重,浸透圧,電解質濃度は,各個体によって相違していることが明らかになりました。


尚,個体RとAの関係については,Naを除き,有意な差が認められませんでした。この理由として,飼育年数,体重,餌料内容が類似していることが推測されましたが,詳しい考察には至りませんでした。今後,検体数の増加により判断できるものと思われます。
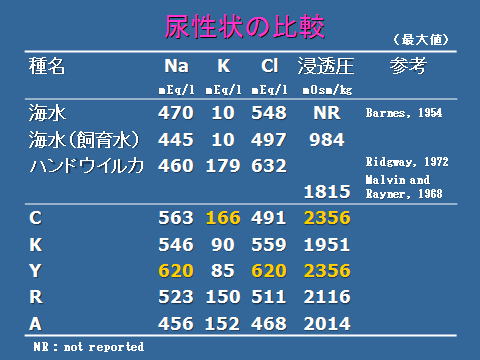
今回得られた数値と,過去の報告から得られているハンドウイルカの尿性状の,Na,K,Cl,浸透圧について比較した結果,Barnes(1954)の報告による海水の濃度,および,当館の飼育水に比べて若干濃い尿を出していることがわかりました.また,ハンドウイルカについては,Ridgway(1972)およびMalvin and Rayner(1968)の報告と同程度の濃度であるという結果が得られました。
今回得られた生理値を,飼育しているハンドウイルカの尿性状の基準値として用いることにより,腎機能や尿路の病気の発見に役立てていくことが出来ます。ただし,検定の結果で見られたように,各生理値は,個体ごとに差異があり,また,これらは,餌料内容や飼育環境により変化することも考えられます。個体ごとにデータを蓄積していくことが望ましいと思われます。
今後も,定期的な尿の採取を継続し,物理的検査,化学的検査で病気の有無を判断すると共に,必要に応じて沈渣の鏡検や,電解質濃度と血液性化学検査を併用するなどの検査を実施していきたいと考えています。
























